Атомы элементов одной группы имеют одинаковое строение внешней электронной оболочки. Именно поэтому такие элементы имеют сходные химические свойства.
Атомы элементов одного периода имеют одинаковое число энергетических уровней.
Периодический закон: «свойства химических элементов, а также образованных ими веществ находятся в периодической зависимости от заряда ядра атома».
Закономерности изменения свойств элементов по группам и периодам:
Увеличивается: заряд, ЭО, окислительные свойства, неметаллические свойства
Уменьшается: радиус, восстановительные свойства, металлические свойства
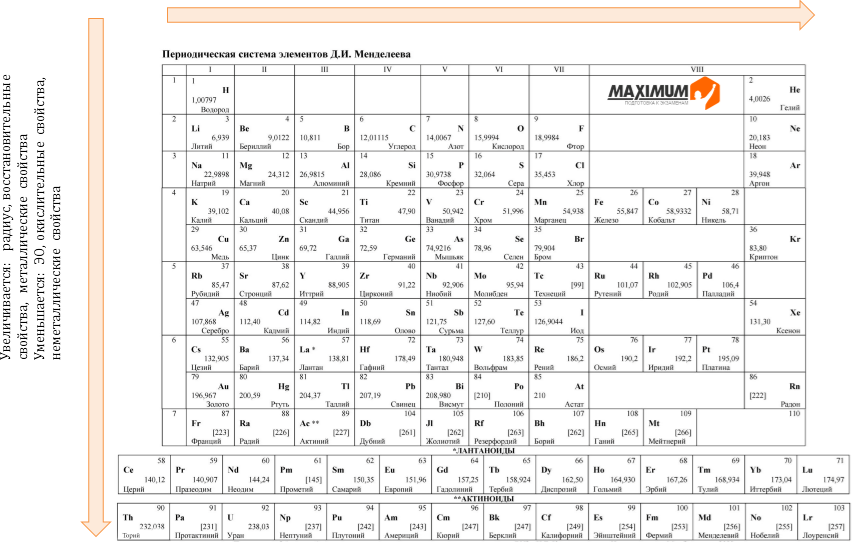
Изменение некоторых характеристик элементов в периодах слева направо:
заряд ядер атомов увеличивается;
радиус атомов уменьшается, потому-что происходит сжатие. Ядру требуется больше энергии, чтобы удержать большое количество электронов, на внешнем уровне;
электроотрицательность элементов увеличивается. (Самый электроотрицательный эелемент – F);
количество валентных электронов увеличивается от 1 до 8 (равно номеру группы);
высшая степень окисления увеличивается (равна номеру группы);
число электронных слоев атомов постоянно, так как это число равно номеру периода;
металлические свойства уменьшаются, так как к концу периода распалагаются неметаллы;
неметаллические элементов увеличивается. (Неметалличность – это способность атомов элемента присоединять электроны).
заряд ядер атомов увеличивается;
радиус атомов увеличивается, потому что увеличивается число электронных слоев;
число энергетических уровней (электронных слоев) атомов увеличивается (равно номеру периода);
число электронов на внешнем слое атомов одинаково (равно номеру группы);
прочность связи электронов внешнего слоя с ядром уменьшается;
электроотрицательность уменьшается;
металличность элементов увеличивается, так как самый типичный металл — это Fr. (Металличность – это способность элемента отдавать электроны);
неметалличность элементов уменьшается.
Элементы, которые находятся в одной подгруппе, являются элементами-аналогами, т. к. они имеют некоторые общие свойства (одинаковую высшую валентность, одинаковые формы оксидов и гидроксидов и др.). Эти общие свойства объясняются строением внешнего электронного слоя.
Электроотрицательностью элемента характеризуется способность его атомов притягивать к себе электроны, которые участвуют в образовании химических связей с другими атомами в молекуле.